问题:
研究氮及其化合物具有重要意义。请回答下列问题:
(1)脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH 3(g) +NO(g) +NO 2(g)  2N 2(g) +3H 2O(g) △H<0,反应的氧化剂是________________。
2N 2(g) +3H 2O(g) △H<0,反应的氧化剂是________________。
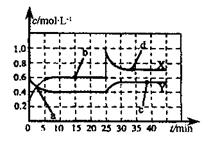
(2)巳知NO 2和N 2O 4可以相互转化:2NO 2(g)  N 2O 4(g) △H<0,现将一定量的混合气体通入一恒温密闭容器中反应,浓度随时间变化关系如图所示。则图中两条曲线X和Y,表示N 2O 4浓度变化的是____,b、c、d三点的化学反应速率大小关系是______;25min时,曲线发生图中变化,可采取的措施是_________。
N 2O 4(g) △H<0,现将一定量的混合气体通入一恒温密闭容器中反应,浓度随时间变化关系如图所示。则图中两条曲线X和Y,表示N 2O 4浓度变化的是____,b、c、d三点的化学反应速率大小关系是______;25min时,曲线发生图中变化,可采取的措施是_________。
(3)25 ℃时,将NH 3溶于水得100 mL0.1 mol • L - 1的氨水,测得pH=11,则该条件下,NH 3 • H 2O的电离平衡常数Kb=_______。
(4)已知:N 2(g)+O 2(g)=2NO(g) △H=+180kJ/mol;
2NO(g)+O 2(g)=2NO 2(g) △H=-112kJ/mol;
2C(s)+O 2(g)=2CO(g) △H=-221kJ/mol;
C(s)+O 2(g)=CO 2 (g) △H=-393.5kJ/mol。
则反应4CO(g)+2NO 2(g)=4CO 2 (g)+ N 2(g) △H=________。
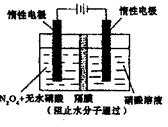
(5)用电化学法可获得N 2O 5。如图装置中,阳极的电极反应式为:N 2O 4+2HNO 3-2e -=2N 2O 5+2H +,则该电解反应的化学方程式为________________。
研究氮及其化合物具有重要意义。请回答下列问题:
(1)脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH 3(g) +NO(g) +NO 2(g) 2N 2(g) +3H 2O(g) △H<0,反应的氧化剂是________________。
2N 2(g) +3H 2O(g) △H<0,反应的氧化剂是________________。
(2)巳知NO 2和N 2O 4可以相互转化:2NO 2(g) N 2O 4(g) △H<0,现将一定量的混合气体通入一恒温密闭容器中反应,浓度随时间变化关系如图所示。则图中两条曲线X和Y,表示N 2O 4浓度变化的是____,b、c、d三点的化学反应速率大小关系是______;25min时,曲线发生图中变化,可采取的措施是_________。
N 2O 4(g) △H<0,现将一定量的混合气体通入一恒温密闭容器中反应,浓度随时间变化关系如图所示。则图中两条曲线X和Y,表示N 2O 4浓度变化的是____,b、c、d三点的化学反应速率大小关系是______;25min时,曲线发生图中变化,可采取的措施是_________。

(3)25 ℃时,将NH 3溶于水得100 mL0.1 mol • L - 1的氨水,测得pH=11,则该条件下,NH 3 • H 2O的电离平衡常数Kb=_______。
(4)已知:N 2(g)+O 2(g)=2NO(g) △H=+180kJ/mol;
2NO(g)+O 2(g)=2NO 2(g) △H=-112kJ/mol;
2C(s)+O 2(g)=2CO(g) △H=-221kJ/mol;
C(s)+O 2(g)=CO 2 (g) △H=-393.5kJ/mol。
则反应4CO(g)+2NO 2(g)=4CO 2 (g)+ N 2(g) △H=________。
(5)用电化学法可获得N 2O 5。如图装置中,阳极的电极反应式为:N 2O 4+2HNO 3-2e -=2N 2O 5+2H +,则该电解反应的化学方程式为________________。

(1)脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH 3(g) +NO(g) +NO 2(g)
 2N 2(g) +3H 2O(g) △H<0,反应的氧化剂是________________。
2N 2(g) +3H 2O(g) △H<0,反应的氧化剂是________________。 (2)巳知NO 2和N 2O 4可以相互转化:2NO 2(g)
 N 2O 4(g) △H<0,现将一定量的混合气体通入一恒温密闭容器中反应,浓度随时间变化关系如图所示。则图中两条曲线X和Y,表示N 2O 4浓度变化的是____,b、c、d三点的化学反应速率大小关系是______;25min时,曲线发生图中变化,可采取的措施是_________。
N 2O 4(g) △H<0,现将一定量的混合气体通入一恒温密闭容器中反应,浓度随时间变化关系如图所示。则图中两条曲线X和Y,表示N 2O 4浓度变化的是____,b、c、d三点的化学反应速率大小关系是______;25min时,曲线发生图中变化,可采取的措施是_________。 
(3)25 ℃时,将NH 3溶于水得100 mL0.1 mol • L - 1的氨水,测得pH=11,则该条件下,NH 3 • H 2O的电离平衡常数Kb=_______。
(4)已知:N 2(g)+O 2(g)=2NO(g) △H=+180kJ/mol;
2NO(g)+O 2(g)=2NO 2(g) △H=-112kJ/mol;
2C(s)+O 2(g)=2CO(g) △H=-221kJ/mol;
C(s)+O 2(g)=CO 2 (g) △H=-393.5kJ/mol。
则反应4CO(g)+2NO 2(g)=4CO 2 (g)+ N 2(g) △H=________。
(5)用电化学法可获得N 2O 5。如图装置中,阳极的电极反应式为:N 2O 4+2HNO 3-2e -=2N 2O 5+2H +,则该电解反应的化学方程式为________________。

参考答案:
