问题:
氨是重要的化工产品和化工原料。
(1)氨的电子式是 。
(2)已知:
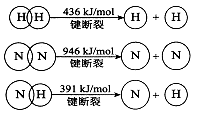
①合成氨的热化学方程式是 。
②降低温度,该反应的化学平衡常数K .(填“增大”、“减小’’或“不变”)。
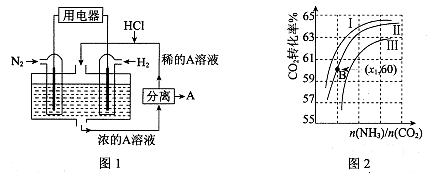
(3)有人设想以N 2和H 2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图l所示。
电池正极的电极反应式是 ,A是 。
(4)用氨合成尿素的反应为2NH 3(g)+CO 2(g)  CO(NH 2) 2(l)+ H 2O(g)。工业生产时,原料气带有水蒸气。图2表示CO 2的转化率与氨碳比
CO(NH 2) 2(l)+ H 2O(g)。工业生产时,原料气带有水蒸气。图2表示CO 2的转化率与氨碳比 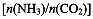 、水碳比
、水碳比 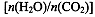 的变化关系。
的变化关系。
①曲线I、II、III对应的水碳比最大的是 。
②测得B点氨的转化率为40%,则x 1 。
氨是重要的化工产品和化工原料。
(1)氨的电子式是 。
(2)已知:

①合成氨的热化学方程式是 。
②降低温度,该反应的化学平衡常数K .(填“增大”、“减小’’或“不变”)。
(3)有人设想以N 2和H 2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图l所示。
电池正极的电极反应式是 ,A是 。

(4)用氨合成尿素的反应为2NH 3(g)+CO 2(g) CO(NH 2) 2(l)+ H 2O(g)。工业生产时,原料气带有水蒸气。图2表示CO 2的转化率与氨碳比
CO(NH 2) 2(l)+ H 2O(g)。工业生产时,原料气带有水蒸气。图2表示CO 2的转化率与氨碳比 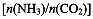 、水碳比
、水碳比 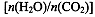 的变化关系。
的变化关系。
①曲线I、II、III对应的水碳比最大的是 。
②测得B点氨的转化率为40%,则x 1 。
(1)氨的电子式是 。
(2)已知:

①合成氨的热化学方程式是 。
②降低温度,该反应的化学平衡常数K .(填“增大”、“减小’’或“不变”)。
(3)有人设想以N 2和H 2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图l所示。
电池正极的电极反应式是 ,A是 。

(4)用氨合成尿素的反应为2NH 3(g)+CO 2(g)
 CO(NH 2) 2(l)+ H 2O(g)。工业生产时,原料气带有水蒸气。图2表示CO 2的转化率与氨碳比
CO(NH 2) 2(l)+ H 2O(g)。工业生产时,原料气带有水蒸气。图2表示CO 2的转化率与氨碳比 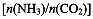 、水碳比
、水碳比 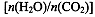 的变化关系。
的变化关系。 ①曲线I、II、III对应的水碳比最大的是 。
②测得B点氨的转化率为40%,则x 1 。
参考答案:
