问题:
CO 2、SO 2、NOx是重要的非金属氧化物,与我们的生存环境息息相关.
(1)SO 2、NOx是形成酸雨和光化学烟雾的环境污染性气体,研究发现,空气中少量的 NO 2能参与硫酸型酸雨的形成,反应过程如下:
①SO 2+NO 2=SO 3+NO ②SO 3+H 2O=H 2SO 4 ③2NO+O 2=2NO 2.
则NO 2在上述过程中的作用与H 2SO 4在下述变化中的作用相似的是______.
A.潮湿的氯气通过盛有浓H 2SO 4的洗气瓶 B.硫化氢通入浓H 2SO 4中
C.亚硫酸钠固体中加入H 2SO 4 D.制备乙酸乙酯时加入浓H 2SO 4
(2)CO 2可用NaOH溶液吸收得到Na 2CO 3或NaHCO 3.
①Na 2CO 3俗称纯碱,因CO 3 2-水解而使其水溶液呈碱性,试写出CO 3 2-水解的离子方程式(忽略第二步水解)______,其水解反应的平衡常数(即水解常数)的表达式为K h=______.
②已知25℃时,K h=2×10 -4mol/L,则当溶液中c(HCO 3 -):c(CO 3 2-)=2:1时,试求溶液的pH=______.
③0.1mol/L Na 2CO 3溶液中c(OH -)-c(H +)=______[用含c(HCO - 3)、c(H 2CO 3)的关系式表示].
(3)汽车尾气的主要成分是一氧化碳和氮氧化物,治理尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)⇌N 2(g)+2CO 2(g);△H<0.
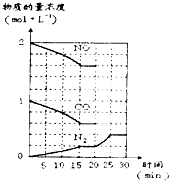
若在一定温度下,将2molNO、lmolCO充入固定容积的容器中,反应过程中各物质的浓度变化如图所示.则从开始到达到平衡状态的过程中,平均反应速率v(CO 2)=______(结果保留两位有效数字).该温度下,反应的化学平衡常数为:K=______(用分数表示).20min时,若改变反应条件,导致N 2浓度发生如图所示的变化,则改变的条件可能是______(填字母).
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO 2的物质的量
A.只有①B.只有②C.只有③D.只有④
CO 2、SO 2、NOx是重要的非金属氧化物,与我们的生存环境息息相关.
(1)SO 2、NOx是形成酸雨和光化学烟雾的环境污染性气体,研究发现,空气中少量的 NO 2能参与硫酸型酸雨的形成,反应过程如下:
①SO 2+NO 2=SO 3+NO ②SO 3+H 2O=H 2SO 4 ③2NO+O 2=2NO 2.
则NO 2在上述过程中的作用与H 2SO 4在下述变化中的作用相似的是______.
A.潮湿的氯气通过盛有浓H 2SO 4的洗气瓶 B.硫化氢通入浓H 2SO 4中
C.亚硫酸钠固体中加入H 2SO 4 D.制备乙酸乙酯时加入浓H 2SO 4
(2)CO 2可用NaOH溶液吸收得到Na 2CO 3或NaHCO 3.
①Na 2CO 3俗称纯碱,因CO 3 2-水解而使其水溶液呈碱性,试写出CO 3 2-水解的离子方程式(忽略第二步水解)______,其水解反应的平衡常数(即水解常数)的表达式为K h=______.
②已知25℃时,K h=2×10 -4mol/L,则当溶液中c(HCO 3 -):c(CO 3 2-)=2:1时,试求溶液的pH=______.
③0.1mol/L Na 2CO 3溶液中c(OH -)-c(H +)=______[用含c(HCO - 3)、c(H 2CO 3)的关系式表示].
(3)汽车尾气的主要成分是一氧化碳和氮氧化物,治理尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)⇌N 2(g)+2CO 2(g);△H<0.
若在一定温度下,将2molNO、lmolCO充入固定容积的容器中,反应过程中各物质的浓度变化如图所示.则从开始到达到平衡状态的过程中,平均反应速率v(CO 2)=______(结果保留两位有效数字).该温度下,反应的化学平衡常数为:K=______(用分数表示).20min时,若改变反应条件,导致N 2浓度发生如图所示的变化,则改变的条件可能是______(填字母).
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO 2的物质的量
A.只有①B.只有②C.只有③D.只有④

(1)SO 2、NOx是形成酸雨和光化学烟雾的环境污染性气体,研究发现,空气中少量的 NO 2能参与硫酸型酸雨的形成,反应过程如下:
①SO 2+NO 2=SO 3+NO ②SO 3+H 2O=H 2SO 4 ③2NO+O 2=2NO 2.
则NO 2在上述过程中的作用与H 2SO 4在下述变化中的作用相似的是______.
A.潮湿的氯气通过盛有浓H 2SO 4的洗气瓶 B.硫化氢通入浓H 2SO 4中
C.亚硫酸钠固体中加入H 2SO 4 D.制备乙酸乙酯时加入浓H 2SO 4
(2)CO 2可用NaOH溶液吸收得到Na 2CO 3或NaHCO 3.
①Na 2CO 3俗称纯碱,因CO 3 2-水解而使其水溶液呈碱性,试写出CO 3 2-水解的离子方程式(忽略第二步水解)______,其水解反应的平衡常数(即水解常数)的表达式为K h=______.
②已知25℃时,K h=2×10 -4mol/L,则当溶液中c(HCO 3 -):c(CO 3 2-)=2:1时,试求溶液的pH=______.
③0.1mol/L Na 2CO 3溶液中c(OH -)-c(H +)=______[用含c(HCO - 3)、c(H 2CO 3)的关系式表示].
(3)汽车尾气的主要成分是一氧化碳和氮氧化物,治理尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)⇌N 2(g)+2CO 2(g);△H<0.
若在一定温度下,将2molNO、lmolCO充入固定容积的容器中,反应过程中各物质的浓度变化如图所示.则从开始到达到平衡状态的过程中,平均反应速率v(CO 2)=______(结果保留两位有效数字).该温度下,反应的化学平衡常数为:K=______(用分数表示).20min时,若改变反应条件,导致N 2浓度发生如图所示的变化,则改变的条件可能是______(填字母).
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO 2的物质的量
A.只有①B.只有②C.只有③D.只有④

参考答案:
