问题:
【题文】(12分)(I)三氧化二铁和氧化亚铜(Cu 2O)都是红色粉末.常用作颜料。已知氧化亚铜溶于稀硫酸生成Cu和CuSO 4。某校化学实验小组为了探究由Fe 2O 3和Cu 2O组成的混合物中两者物质的量相对大小,某同学认为只要取少量粉末放入足量稀硫酸中,通过观察现象即可。
(1)上述实验过程中发生的反应有(用离子方程式表示):
①Fe 2O 3+6H += 2Fe 3++3H 2O
② ③
(2)若实验中观察到溶液变为蓝色且有固体剩余,则n(Cu 2O) n(Fe 2O 3)。(填“>”、“<”或“=”)。
(II)分别在密闭容器的两个反应室中进行如下反应:
左反应室:A(g)+2B(g) 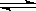 2C(g)
2C(g)
右反应室:2Z(g) 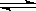 X(g)+Y(g)
X(g)+Y(g)
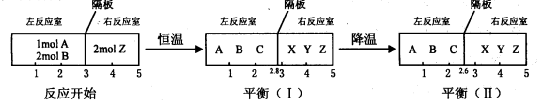
在反应室之间有无摩擦、可自由滑动的密封板隔断。反应开始和达到平衡时有关物理量的变化如下图所示:
(1)A(g)+2B(g) 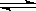 2C(g) 的△H 0(填“>”、“<”或“=”)。
2C(g) 的△H 0(填“>”、“<”或“=”)。
(2)在平衡(I)和平衡(Ⅱ)中,X的体积分数 (填序号)。
a.一定相等 b.一定不相等 c.可能相等
(3)达到平衡(I)时,A的转化率为 。
【题文】(12分)(I)三氧化二铁和氧化亚铜(Cu 2O)都是红色粉末.常用作颜料。已知氧化亚铜溶于稀硫酸生成Cu和CuSO 4。某校化学实验小组为了探究由Fe 2O 3和Cu 2O组成的混合物中两者物质的量相对大小,某同学认为只要取少量粉末放入足量稀硫酸中,通过观察现象即可。
(1)上述实验过程中发生的反应有(用离子方程式表示):
①Fe 2O 3+6H += 2Fe 3++3H 2O
② ③
(2)若实验中观察到溶液变为蓝色且有固体剩余,则n(Cu 2O) n(Fe 2O 3)。(填“>”、“<”或“=”)。
(II)分别在密闭容器的两个反应室中进行如下反应:
左反应室:A(g)+2B(g)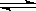 2C(g)
2C(g)
右反应室:2Z(g)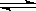 X(g)+Y(g)
X(g)+Y(g)
在反应室之间有无摩擦、可自由滑动的密封板隔断。反应开始和达到平衡时有关物理量的变化如下图所示:

(1)A(g)+2B(g)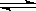 2C(g) 的△H 0(填“>”、“<”或“=”)。
2C(g) 的△H 0(填“>”、“<”或“=”)。
(2)在平衡(I)和平衡(Ⅱ)中,X的体积分数 (填序号)。
a.一定相等 b.一定不相等 c.可能相等
(3)达到平衡(I)时,A的转化率为 。
(1)上述实验过程中发生的反应有(用离子方程式表示):
①Fe 2O 3+6H += 2Fe 3++3H 2O
② ③
(2)若实验中观察到溶液变为蓝色且有固体剩余,则n(Cu 2O) n(Fe 2O 3)。(填“>”、“<”或“=”)。
(II)分别在密闭容器的两个反应室中进行如下反应:
左反应室:A(g)+2B(g)
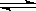 2C(g)
2C(g) 右反应室:2Z(g)
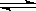 X(g)+Y(g)
X(g)+Y(g) 在反应室之间有无摩擦、可自由滑动的密封板隔断。反应开始和达到平衡时有关物理量的变化如下图所示:

(1)A(g)+2B(g)
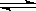 2C(g) 的△H 0(填“>”、“<”或“=”)。
2C(g) 的△H 0(填“>”、“<”或“=”)。 (2)在平衡(I)和平衡(Ⅱ)中,X的体积分数 (填序号)。
a.一定相等 b.一定不相等 c.可能相等
(3)达到平衡(I)时,A的转化率为 。
参考答案:
