问题:
(14分)氯化铜晶体(CuCl 2· xH 2O)是重要的化工原料,可用作催化剂、消毒剂等。用孔雀石[主要含Cu 2(OH) 2CO 3,还含少量Fe、Si的化合物]制备氯化铜晶体,方案如下:
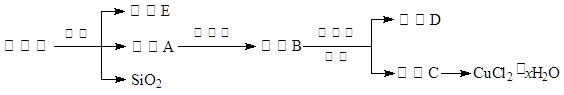
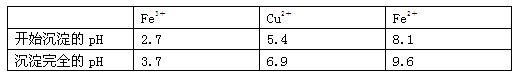
已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
⑴酸溶时,为了提高浸取率可采取的措施有 。(写出一点)
⑵若溶液A含有的金属离子有Cu 2 +、Fe 2 +,则试剂①为Cl 2,通入Cl 2发生反应的离子方程式: 。
⑶加入试剂②的目的是调节pH至 a, a的范围是 ;
为避免引入杂质离子,试剂②可选用 。
A.氨水
B.氧化铜
C.氢氧化铜
D.氢氧化钠
⑷由溶液C获得CuCl 2· xH 2O,实验操作依次是加热浓缩、冷却结晶、过滤和洗涤等操作。加热浓缩过程需加入少量盐酸的目的是: 。
⑸工业生产过程会产生含Cu 2 +的废水,向废水加入碱调节pH=8,沉降后废水中Cu 2 +浓度为 mol/L。(已知 Ksp[Cu(OH) 2]=5.6×10 -20)
⑹氯化亚铜(CuCl)也是一种重要的化工原料。
制备过程:向CuCl 2溶液中通入一定量的SO 2,加热一段时间后生成CuCl白色沉淀。写出制备CuCl的离子方程式: 。
(14分)氯化铜晶体(CuCl 2· xH 2O)是重要的化工原料,可用作催化剂、消毒剂等。用孔雀石[主要含Cu 2(OH) 2CO 3,还含少量Fe、Si的化合物]制备氯化铜晶体,方案如下:
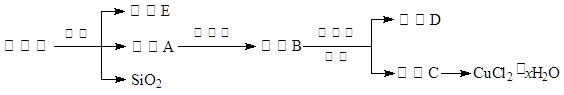
已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:

⑴酸溶时,为了提高浸取率可采取的措施有 。(写出一点)
⑵若溶液A含有的金属离子有Cu 2 +、Fe 2 +,则试剂①为Cl 2,通入Cl 2发生反应的离子方程式: 。
⑶加入试剂②的目的是调节pH至 a, a的范围是 ;
为避免引入杂质离子,试剂②可选用 。
⑷由溶液C获得CuCl 2· xH 2O,实验操作依次是加热浓缩、冷却结晶、过滤和洗涤等操作。加热浓缩过程需加入少量盐酸的目的是: 。
⑸工业生产过程会产生含Cu 2 +的废水,向废水加入碱调节pH=8,沉降后废水中Cu 2 +浓度为 mol/L。(已知 Ksp[Cu(OH) 2]=5.6×10 -20)
⑹氯化亚铜(CuCl)也是一种重要的化工原料。
制备过程:向CuCl 2溶液中通入一定量的SO 2,加热一段时间后生成CuCl白色沉淀。写出制备CuCl的离子方程式: 。
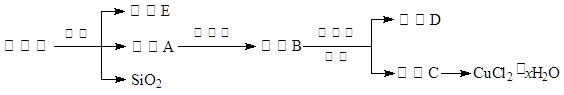
已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:

⑴酸溶时,为了提高浸取率可采取的措施有 。(写出一点)
⑵若溶液A含有的金属离子有Cu 2 +、Fe 2 +,则试剂①为Cl 2,通入Cl 2发生反应的离子方程式: 。
⑶加入试剂②的目的是调节pH至 a, a的范围是 ;
为避免引入杂质离子,试剂②可选用 。
| A.氨水 | B.氧化铜 | C.氢氧化铜 | D.氢氧化钠 |
⑸工业生产过程会产生含Cu 2 +的废水,向废水加入碱调节pH=8,沉降后废水中Cu 2 +浓度为 mol/L。(已知 Ksp[Cu(OH) 2]=5.6×10 -20)
⑹氯化亚铜(CuCl)也是一种重要的化工原料。
制备过程:向CuCl 2溶液中通入一定量的SO 2,加热一段时间后生成CuCl白色沉淀。写出制备CuCl的离子方程式: 。
参考答案:
